МАТЕРИАЛЫ ПО ЭКОЛОГИИ
Гигиенические критерии состояния окружающей среды для полихлорированных бифенилов и терфенилов
22 мая 2009 г.
7. ЭКСПЕРИМЕНТАЛЬНОЕ ИЗУЧЕНИЕ ВОЗДЕЙСТВИЯ ПХБФ И ПХТФ
7.1 Токсическое воздействие на различные виды
Большинство имеющейся информации о токсичности ПХБФ получено из исследований, выполненных с коммерческими смесями. Значительно меньший объем доступной информации,. посвященной примесям в коммерческих продуктах и ПХТФ, приведен в разделах 7.2 и 7.3.
7.1.1 Млекопитающие
7.1.1.1 Острая токсичность при скармливании и внутривенном введении
Ранние работы, выполненные Monsanto Company, показали низкую острую токсичность при скармливании Арохлора, при этом LD50S для крыс варьировало от 4.0 г/кг лля Аоохлора 1221 до 11,3 г/кг для Арохлора 1262 (Panel on Hazardous Trace Substances, 1972). Недавние работы продемонстрировали несколько более высокую токсичность (Bruckner et al., 1973; Grant и Philips, 1974). При введении единичной внутривенной дозы LD50 для Арохлора 1254 оказалась равной 358 мг/кг массы тела взрослых самок крыс линии Шерман (binder et al., 1974). Острая оральная LD5o Арохлора 1254 для крыс у той же линии и пола оказалась в пределах 4-10 г/кг (Kim-brough et al., 1972). По данным Bruckner и др. (1973), у сильно затравленных животных наблюдается быстрая потеря массы тела, атаксия, диарея и хромодакриорея и они гибнут от прогрессирующей дегидратации и поражения центральной нервной системы. У таких крыс наблюдалась вакуолизация печени и почек (Bruckner et al., 1973), а также изъязвление слизистой оболочки желудка и 12-перстной кишки (Kimbro-ugh et al., 1972).
Yamamoto и Yoshimura (1973) обнаружили, что интрапери-тонеальная LD50 2,4,3',4/-тетрахлорбифенила для мышей составляет 2,15 г/кг массы тела и что LD50 5-оксипроизводного,, который является главным метаболитом in vivo, оказалось равной 0,43 г/кг массы тела.
7.1.1.2 Подострая токсичность при скармливании
После повторного выделения ПХБФ проявляет кумулятивное токсическое действие. В группе крыс, получавших с кормом Арохлор 1254 в концентрации 1 г/кг, смерть наступала между 28-м и 53-м днями кормления (Tucker и Grabtree, 1970), а при применении фенохлора ДР6 в концентрации 2 г/гк - между 12-м и 26-м днем кормления (Vos и Koeman,. 1970). В последнем эксперименте на вскрытии отмечалось увеличение печени, уменьшение селезенки и прогрессирующая гепатопорфирия химической этиологии. Повторное еженедельное скармливание 150 мг Арохлора 1221, 1242 или 1254 кроликам в течение 14 нед приводило к увеличению печени и ее повреждению в случае Арохлора 1242. При использовании Арохлора 1221 не было отмечено никакого эффекта (Koller и Zinkl, 1973). Allen и др. (1974) скармливали 6 самкам обезьян резус в течение 2 мес диету, содержащую Арохлор 1248 в концентрации 25 мг/кг; у животных по прошествии 1 мес наблюдался отек лица, потеря волос и акне, и одна обезьяна погибла от тяжелого гастрита через 2 мес после прекращения скармливания экспериментального рациона. Содержание ПХБФ в жире тела животных после 2 мес воздействия в среднем составляло 127 мг/кг, в то время как через 8 мес это значение уменьшилось до 34 мг/кг.
Норки оказались необычно чувствительными к ПХБФ. Aulerich и др. (1973) скармливали рацион, содержавший ПХБФ в концентрации 30 мг/кг (по 10 мг/кг Арохлора 1242, 1248 и 1254), взрослым норкам, что привело к 100%-й смертности в течение 6 мес. Остаточные количества ПХБФ в мозге этих норок составляли в среднем около 11 мг/кг и были примерно вдвое выше уровней, наблюдавшихся в других тканях. Скармливание Арохлора 1254 норкам в концентрации 5 и 10 мг/кг в течение 4 мес сопровождалось зависимым от дозы замедлением прибавки в массе тела растущих самок. Самки норки, получавшие с кормом Арохлор 1254 в концентрации 5 мг/кг в течение 9 мес, оказались неспособными к воспроизведению потомства (Ringer et al., 1972).
7.1.1.3 Хроническая токсичность пои скармливании
Арохлор 1242, 1254 и 1260 скармливали крысам в течение 18 мес в концентрации 1, 10 и 100 мг/кг (Keplinger et al., 1971). При использовании концентрации 10 мг/кг никаких неблагоприятных эффектов не наблюдалось, однако при применении Арохлора 1242 и 1254 в концентрации 100 мг/кг имело место увеличение массы печени и уменьшение выживаемости потомства. В подобных экспериментах, поставленных на собаках, было отмечено понижение прибавки массы тела при скармливании Арохлора 1254 и 1260 в концентрации 100 мг/кг (Keplinger et al., 1971). В экспериментах Kimbrough и др. (1972) самцы крыс выживали при добавлении Арохлора 1260 к рациону в концентрации 1 г/кг (71,4 мг/кг массы тела) в течение 8 мес, однако от такой дозы погибло 8/10 самок; 2/10 самок погибли при концентрации 500 мг/кг и 1/10 - 100 мг/кг (7,2 мг/кг массы тела). При скармливании Арохлора 1254 и 1260 увеличение массы печени в зависимости от концентрации у самцов крыс было существенным вплоть до концентрации 20 мг/кг (1,4 мг/кг массы тела); у самок увеличение печени встречалось только при увеличении концентрации ПХБФ в рационе до 500 мг/кг и выше. Пораженная печень характеризовалась оранжевой флюоресценцией, клетки печени были увеличенными с наличием в них вакуолей и жировых включений; отмечалось также усиление ретикулярной структуры эндоплазмы и наличие аденофиброза, которые были более выраженными при использовании Арохлора 1254 (см. раздел 7.8). Grant и др. (1974) скармливали рацион, содержащий Арохлор 1254 в концентрациях 0, 2, 20 и 100 мг/кг, крысам в течение 246 дней, после чего крысы содержались еще 180 дней на диете, свободной от ПХБФ. Через 246 дней масса тела крыс, получавших корм с концентрацией Арохлора 1254 100 мг/кг, оказалась значительно меньшей, чем у контрольных животных, а масса печени большей. Наиболее заметным изменением печени при гистологическом исследовании было появление жировых микровключений в централобулярной области; этот эффект оказался зависимым от величины затравочной дозы, не наблюдался у крыс, получавших с кормом ПХБФ в концентрации 2 мг/кг. Эффект оказался обратимым при переходе крыс на обычный рацион.
Увеличение печени наблюдал ряд авторов у различных видов животных при применении различных смесей и чистых изомеров ПХБФ, причем этот эффект приписывался главным образом гипертрофии тонкой эндоплазматической ретикулярной структуры печеночных клеток (Vos и Beems, 1971; Allen et al., 1973; Kimbrough, 1974; Nishizumi, 1970), но при достаточно высоких дозах (пероральное введение доз порядка 150 мг/кг массы тела/нед в течение 14 нед) Арохлора 1254 и 1242 указанные изменения прогрессировали вплоть до выраженного повреждения печени (Koller, Zinkl, 1973). Тонкая эндоплазматическая ретикулярная структура печеночных клеток может уплотняться и образовывать гиалиновые включения. Этот процесс может сопровождаться потерей ферментативной активности этого образования. При этом тоже могут наблюдаться скопления липидов, отложение пигмента, изменения в ядрах клеток и некроз печеночных клеток (Vos и Notenboom-Ram, 1972).
Обезьяны резус оказались единственным видом, на котором удалось продемонстрировать признаки отравления, сходные с наблюдавшимися у пациентов с болезнью Юшо (см. раздел 8). Скармливание Арохлора 1248 в концентрации 2,5 и 5,0 мг/гк в течение 1 г. вызвало появление периорбитального отека, алопецию, эритему и акнеиформные поражения кожи в области лица и шеи в пределах 1-2 мес. Эти проявления были менее заметными у обезьян-самцов. При скармливании Арохлора 1248 в концентрации 25 мг/кг одна обезьяна из группы в 6 животных погибла, в то время как при скармливании его в концентрации 100 и 300 мг/кг смертность достигла 100% в течение 2-3 мес. У животных, подвергшихся более тяжким воздействиям, наблюдались проявления гипертрофического гиперпластического гастрита с изъязвлениями, анемия, гиперпротеинемия и гипоплазия костного мозга. У выживших животных симптомы отравления наблюдались 8 мес спустя после воздействия (Allen и Norback, 1973; Allen et al., 1974; Allen, 1975).
7.1.1.4 Токсичность при попадании на кожу
Vos и Beems (1971) подтвердили данные, полученные в ранних работах, о том, что ПХБФ повреждает фолликулярный эпителий у экспериментальных животных. Они наносили 3 коммерческих смеси препаратов 60% уровня хлорирования, а именно Хлофен А60, Фенохлор ДР6 и Арохлор 1260 на кожу кроликов, ежедневно в дозе 118 мг/50 см2 (5 раз в неделю) в течение 38 дней. После первоначального покраснения развивалась поперечноисчерченная морщинистость с гиперплазией и гиперкератозом как эпидермального, так и фолликулярного эпителия. Этот эффект был более заметен при использовании Хлофена и Фенохлора, чем при применении Арохлора.
В ходе этих экспериментов гибель животных наблюдалась в группах, обработанных Хлофеном и Фенохлором, но не в группах, получавших Арохлор. Повреждения почек наблюдались во всех группах; повреждения печени были наименьшими в группах, получавших Арохлор. Наблюдалась атрофия корковой зоны тимуса и уменьшение числа зародышевых центров лимфатических узлов, так же как и появление лимфопенин, а у некоторых животных во всех группах - отечные явления в брюшной и грудной полостях, в подкожной жировой ткани и перикарде. Выделение копро- и протопорфиринов с фекалиями возросло при воздействии всех трех видов ПХБФ, будучи наименьшим при использовании Арохлора 1260. Vos и Beems отнесли большую тяжесть проявлений, наблюдавшихся при воздействии Хлофена и Фенохлора, за счет присутствия в них токсических примесей (см. раздел 7.2). В другом сравнительном исследовании токсичности на кроликах (Vos и No-tenboom-Ram, 1972), кожные поражения у животных, подвергавшихся воздействию Арохлора 1260, были менее тяжелыми, чем у животных, обработанных 2,4,5,2',4',5/-гексахлорбифени-лом. В одном из японских исследований никакой разницы в кожных поражениях при нанесении на кожу кроликов Канехлора 400, Канехлора 500 или 3,4,3',4'-тетрахлорбифени-ла обнаружено не было (Komatsu и Kikuchi, 1972).
7.1.1.5 Токсичность при ингаляции
Опубликовано только одно исследование, посвященное ингаляции Арохлора 1242 и 1254 (Treon et al., 1956). Крысы, мыши, кролики и морские свинки подвергались воздействию' паров Арохлора 1242 или 1254 в течение 5 дней в неделю, опыты продолжались несколько недель при использовании концентраций в пределах 1,5-8,6 мг/м3. При таких концентрациях Арохлор 1254 вызвал увеличение печени у крыс.
7.1.2 Птицы
Общая токсичность при поедании с кормом Арохлора 1242 и 1254 оказалась низкой для диких уток, при этом LD50 оказалась большей, чем 2 г/кг массы тела (Tucker и Grabtree, 1970). Цифры летальных доз, опубликованные в литературе, для птиц, подвергавшихся повторному воздействию, весьма вариабельны; очевидно, что летальные дозы зависят от вида, возраста птицы, метода введения, степени хлорирования ПХБФ и наличия в них примесей (Vos, 1972). Heath и др. (1970) определили необходимые концентрации Арохлора 1232 и 1262 в корме, которые при скармливании более чем в течение 5 дней могут погубить 50% взятых в опыт диких уток, фазанов или куропаток. Концентрации препаратов находились в пределах от 500 до более чем 5000 мг/кг, при этом короткохвостая белая куропатка оказалась наиболее, а японская куропатка наименее чувствительной к указанному воздействию. Имела место положительная корреляция между процентом содержания хлора в техническом Аро-хлоре и его токсичностью. Эта взаимосвязь оставалась справедливой и для соединений, содержащих менее 60% хлора, - Арохлора 1260 и 1262, мало отличающихся друг от друга. Реакции со стороны организма диких уток оказались менее зависимыми от содержания хлора в препаратах, чем у трех видов семейства куриных. Prestt и др. (1970) обнаружили 50% смертность среди бенгальских лесных певчих птиц, получавших суточную пероральную дозу Арохлора 1254, равную 254 мг/кг массы тела, в течение 56 дней; бакланы погибали при накоплении у них кумулятивной дозы Хлофена А60, равной 5,7 г, в то время как цапли оказались более устойчивыми (Koeman et al., 1973).
Токсичность корма, содержащего Фенохлор ДР6, Хлофен А60 или Арохлор 1260 в дозе 400 мг/кг, для цыплят изучалась Vos и Koeman (1970). Первые два препарата вызвали 100% смертность через 24,3 и 20,5 дней, тогда как Арохлор вызывал только 15% смертность, причем за более чем 60-дневный срок. Авторы показали присутствие примесей в Фенохлоре и Хлофене (Vos et al., 1970). Результаты Flick и др. (1965) и Platonow, Funnel (1971) показали, что цыплята могут выживать при поедании с кормом Арохлора 1248 в концентрации 200 мг/кг в течение нескольких месяцев и что гибель цыплят может наступить при увеличении указанной концентрации до 250 мг/кг, в то время как Rehfeld и др. (1971) обнаружили у него более высокую токсичность, зарегистрировав 1/30 случаев смерти при использовании в концентрации 30 мг/кг свыше 25 дней и 16/30 в концентрации 50 мг/кг. Keplinger и др. (1971) обнаружили замедление роста цыплят, получавших Арохлор 1252 с кормом в концентрации 10 мг/кг и Арохлор 1254 в концентрации 10 мг/кг, при отсутствии влияния потребления с кормом Арохлора 1260 в концентрации 100 мг/кг. У птиц с тяжелым отравлением ПХБФ наблюдается тремор, атаксия, взъерошенный вид и потеря перьев. Отек в брюшной и плевральной полостях являлся характерным признаком, наблюдавшимся при аутопсии в ряде экспериментов (Flick et al., 1965) у очень большого количества цыплят, погибших в результате контаминации корма в Японии Кане-хлором КС 400 (Kohanawa et al., 1969 a, 1969 b). Иногда у пораженных птиц имеется увеличение почек и печени; некоторые авторы отмечают уменьшение селезенки, гребня и яичек, увеличение надпочечников, щитовидной железы и поблед-нение поджелудочной железы. Не наблюдалось никаких патологических признаков Dahlgren et al. (1972), которые могли бы выступать в качестве причины гибели фазанов в результате поглощения кумулятивной дозы Арохлора 1254 порядка 900 мг (ежедневное поглощение с кормом от 20 до 200 мг самками 11-недельного возраста); средняя концентрация в мозговой ткани фазанов после гибели составляла 520 мг/кг; в данном случае нельзя исключить решающей роли поражения центральной нервной системы.
7.1.3 Водные организмы
7.1.3.1 Рыба
Stalling и Mayer (1972) сообщили, что оральная LD50 Арохлора 1242 и 1260 для радужной форели составляет более 1,5 мг/кг. Доза 15 мг/кг при скармливании треске нарушала ее способность поддерживать вертикальное положение в бурной воде (Lindahl, неопубликованный доклад, 1974).
Определение токсичности для рыб путем добавления ПХБФ в аквариумную воду является источником значительных ошибок вследствие различной растворимости компонентов. Zitko (1970) показал, что растворимость в воде Арохлора 1221 составляет 3,8-5 мг/л и Арохлора 1254 0,3-0,5 мг/л. По данным Stalling и Mayer (1972), 4-дневные LC50 для форели составляют 1,17 мг/л (Арохлор 1221) и вплоть до 60 мг/л (Арохлор 1260); в данном случае данные о растворимости явно преувеличены. В более продолжительных экспериментах этих авторов (табл. 8) большинство концентраций находилось в пределах растворимости и поэтому эти данные более надежны. В длительных экспериментах Hansen и др. (1971) обнаружили гибель рыбы, подвергавшейся воздействию Арохлора 1254 в течение 45 дней в концентрации 5 мкг/л, но не 1 мкг/л. Эти результаты показывают, что действие ПХБФ на рыбу носит кумулятивный характер и что их токсичность уменьшается по мере возрастания степени хлорирования препаратов.
Таблица 8. Биологические тесты по выявлению действия прерывистых потоков различных Арохлоров на 3 вида рыб
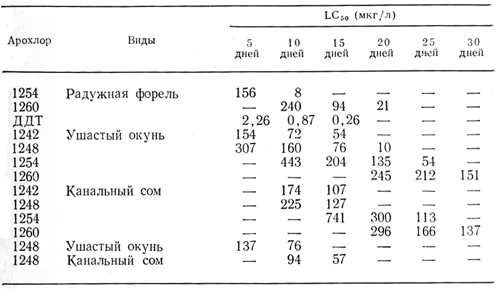
Молодые особи рыбы более чувствительны к ПХБФ, чем взрослые; 96-часовые LD50 для мальков черноголовой пиме-фалес составляли для Арохлора 1242 и 1254 и 8 мкг/л соответственно. Рост мальков черноголовой пимефалес и кулии нарушался при концентрациях этих препаратов в воде, превышающих 2,2 мкг/л (Nebeker et al., 1974). Информация о патологических изменениях у рыб под воздействием летальных концентраций ПХБФ отсутствует. Hansen и др. (1971) показали, что рыба выдерживает воздействие Арохлора 1254 в концентрации 5 мкг/л, погибая после возвращения в чистую воду при наличии признаков понижения сопротивляемости к инфекциям. У радужной форели, которой скармливали Арохлор 1254 в концентрации 10 и 100 мг/кг в течение 330 дней, наблюдались патологические изменения в почках, селезенке и печени (Nestel и Budd, 1975).
7.1.3.2 Водные беспозвоночные
Результаты нескольких работ по определению токсичности ПХБФ для водных беспозвоночных были опубликованы Stalling и Mayer (1972). Экспозиция разнообразных рачков (Gammarus pseudolimnaeus) к воздействию ПХБФ показала, что их токсичность уменьшается по мере увеличения степени хлорирования; были получены 4-дневные LC50 для Арохлора 1242, 1248 и 1254, равные 10, 52 и 2400 мкг/л соответственно-Пороговая концентрация для выживания, роста и осуществления репродукционной функции Gammarus pseudolimnaeus, экспонированных к воздействию Арохлора 1248, составляла около 5 мкг/л, будучи той же самой для Daphnia magna. Что касается речных раков, 7-дневная LC50 для них составляла 30 мкг/л (Арохлор 1242) и 80 мкг/л (Арохлор 1254) и для чилимов - 3 мкг/л (Арохлор 1254). Wildish (1970) показал, что смертность среди Gammarus oceanicus зависела от длительности экспозиции к Арохлору 1254 при концентрациях, превышающих 10 мкг/л. Stalling и Mayer (1972) сообщили, что 15-дневная LC5o Арохлора 1254 при экспозиции незрелых чилимов составляет 0,94 мкг/л.
7.1.3.3 Микроорганизмы
Рост некоторых морских диатомовых водорослей подавляется Арохлором 1254 при концентрации 10-25 мкг/л; морские и пресноводные водоросли более устойчивы и выдерживают концентрации Арохлора 1254 порядка 100 мкг/л (Mosser et al., 1972). Fisher et al. (1972) показали, что фитопланктон Саргассова моря не растет при концентрациях Арохлора 1254 10 мкг/л, хотя фитопланктон лиманов и прибрежных вод не так сильно повреждается при такой концентрации. Keil и др. (1971) сообщили, что рост диатомовых водорослей подавлялся Арохлором 1242 в концентрации 100 мкг/л с уменьшением синтеза в них рибонуклеиновой кислоты; при концентрации 10 мгк/л указанный эффект не наблюдался.
Рост культур озерных бактерий не подавлялся Арохлором 1221, 1242 и 1254 при избыточной их растворимости; Арохлор 1221 и 1242 может использоваться такими бактериями в качестве источника углерода и энергии (Wong и Kaiser, 1975).
7.2 Токсичность примесей, содержащихся в коммерческих ПХБФ
Vos и Koeman (1970) обнаружили, что Фенохлор DP6 и Хлофен А60 более токсичны для цыплят, чем Арохлор 1260 (см. раздел 7.1.2). Vos и Beems (1971) сообщили о подобных различиях в дермальной токсичности этих препаратов для кроликов (см. раздел 7.1.1.4). Vos и др. (1970) разделили Хлофен А60 и Фенохлор DP6 на неполярные и ПХБФ и их полярные фракции и обнаружили полярные компоненты, которые дотоле не выявлялись в подобной фракции Арохлора 1260. Фенохлор DP6, Хлофен А60 и полярная фракция Хло-фека А60 вызвали высокую смертность куриных эмбрионов, в то время как полярная фракция Арохлора 1260 этими свойствами не обладала. Различия между этими тремя фракциями были также показаны на примере развития кожных поражений у кроликов (Vos и Beems, 1971). Масс-спектрографический анализ показал, что в качестве примесей ПХБФ выступают тетра- и пентахлордибензофураны. Дополнительными загрязнителями коммерческих препаратов являются хлорированные нафталины. Vos и др. (1970) подсчитали, что максимальный уровень хлорированных дибензофуранов в Хлофе-не А60 составляет 5 мг/кг и в Фенохлоре DP6 - 20 мг/кг. Они показали, что хлорированные дибензофураны примерно на один порядок менее токсичны, чем хлорированные бензодиоксины, и пришли к заключению, что эти вещества в основном ответственны за общую токсичность полярных фракций и за различия в токсичности между тремя указанными коммерческими смесями ПХБФ.
В последнее время хлорированные дибензофураны были обнаружены в рисовом масле, контаминированном ПХБФ, которое было ответственно за появление болезни Юшо в Японии (см. раздел 8, с. 75).
В 1961 г. Bauer и др. продемонстрировали токсичность смеси, состоящей из три- и тетрахлорбензофуранов: однократная оральная доза в 0,5-1,0 мг/кг массы тела вызывала тяжелые и зачастую летальные некрозы печени у кроликов. При нанесении смеси на кожу уха кролика появлялась гиперплазия и гиперкератоз. Подобные токсические эффекты были обнаружены при использовании 2,3,7,8-тетрахлордибензо-р-диоксина в дозах, которые были в 10 раз меньшими тех, которые оказались токсичными в случае применения хлорированных дибензофуранов. [Смотри также обзор FJmbrough (1974).] 2,3,7,8-Тетрахлордибензофуран, который, как недавно было показано, присутствует в ПХБФ (Bowes et al., 1975), вызвал гибель цыплят после 8-15-дневного поглощения оральной дозы препарата 5 мкг/кг/день. Однократная оральная доза в 4000 мкг/кг оказалась несмертельной для мышей. Порфирия не наблюдалась ни у цыплят, ни у мышей (Goldstein et al., 1975a). В то же время 8 из 10 цыплят погибли после 9-13-дневного поглощения с кормом оральной дозы 2,3,7,8-тетрахлордибензо-р-диоксина 1 мкг/кг массы тела/день (Schwetz et al., 1975). Оральная LD50 2,3,7,8-тетрахлордибек-зофурана для морских свинок составляет примерно 7 мкг/кг массы тела, что почти на один порядок больше аналогичной токсичности 2,3,7,8-тетрахлордибензо-р-диоксина (Moore, 1975).
Используя масс-спектрометрию с низким разрешением, МсКдппеу (1975) обнаружил метаболиты в выделениях цыплят, которым скармливали 2,4,6,2'4,6'-гексахлорбифенил, содержавший эталонные массы хлордибензофуранов. Кроме того, с помощью перхлорирования он идентифицировал окта-хлордибензофуран. используя тот же метод масс-спектрометрии с низким разрешением. 2,4,6,2',4',6/-гексахлорбифениловый изомер в коммерческих смесях обнаружен не был.
Zitko и др. (1972b) пытались обнаружить присутствие хлорированных дибензофуранов в рыбе и рыбных продуктах из контаминированных прибрежных зон. Образцы включали в себя ткани акул, яйца бакланов и серебристых чаек, жир сельди и сельдяную муку. Чувствительность метода составляла 0,01-0,02 мг/кг. Хлорированные дибензофураны при этом обнаружены не были. Авторы признали, что чувствительность метода была недостаточно высокой, чтобы обнаружить количества указанных соединений, которые могут оказать выраженное токсическое действие. Curley и др. (1975) обнаружили компонент, который имел четыреххлористую изотопную группу и массовое число 304, соответствующее массовому числу тетрахлордибензофурана в моче крыс, подвергавшихся воздействию ПХБФ, однако полной идентификации в этом случае проведено не было.
7.3 Токсичность ПХТФ
Систематического изучения токсичности ПХТФ не проводилось. Sosa-Lucero и др. (1973) скармливали группам крыс в течение 7 дней Арохлор 5460 в концентрации 0, 10, 100 и 1000 мг/кг. При этом отрицательного воздействия на здоровье и массу тела обнаружено не было; выраженное увеличение печени было зарегистрировано при использовании концентрации 1000 мг/кг. При проведении испытания на эстрогенную активность, включавшего получение ответной реакции незрелой матки крысы на гликоген, Арохлор 5460 оказался неактивным, так же как и Арохлор 1260; Арохлор 5442 был более активным, чем Арохлор 1242 (Bitman et al., 1972). Поглощение Арохлора 5460 с кормом в концентрации 5000 мг/кг в течение 12 нед вызвало уменьшение массы тела и увеличение массы печени у обезьян резус (Allen и Norback, 1973); по прошествии 6 нед у животных наблюдались отечность лица, выпадение волос и выделения из глаз, подобные тому, что наблюдались теми же авторами в экспериментах с Арохлором 1248 (раздел 7.1.1.2), при наличии аналогичных изменений в желудке.
7.4 Биохимические эффекты
7.4.1 Индукция ферментов
Многие исследователи наблюдали усиление эндоплазмати-ческих ретикулярных структур печеночных клеток после воздействия ПХБФ (см. раздел 7.1.1.3). Этот феномен обычно сопровождался индукцией микросомной оксидазы со смешанной функцией. Индукция микросомной ферментативной активности подобно увеличению печени более выражена при воздействии высокохлорированных ПХБФ и относительно низка при использовании Арохлора 1221 и 1016 (Villeneuve et al., 1971а, 1972; Bickers et al., 1972; Ecobichon и Comeau, 1974). Этот эффект был также продемонстрирован при однократном введении оральной дозы чистых ПХБФ (Fujita et al., 1971); сравнительно недавно эти работы были подтверждены John-stone и др. (1974), чьи результаты суммированы в табл. 9, демонстрируя высокую степень индукции ферментов при воздействии высокохлорированных соединении.
Таблица 9. Стимуляция микросомной ферментативной активности отдельными хлорированными бифенилами
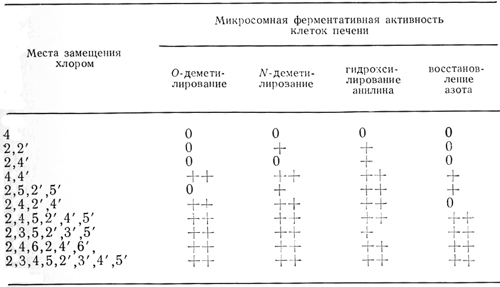
Grant и др. (1974) обнаружили увеличение микросомной ферментативной активности у крыс, получавших Арохлор 1254 в концентрации 20 мг/кг с кормом в течение 246 дней, но не в концентрации 2 мг/кг. Iverson и др. (1975) и Goldstein et. al. (1975) сравнивали индуцирующий потенциал микросомной ферментативной активности Арохлора 1242 и 1016. Iverson и др. (1975) обнаружили повышение печеночной мик-росомальной ферментативной активности под воздействием обоих типов Арохлора у самцов крыс, получавших в течение 21 дня рацион, содержавший дозу 1 мг/кг массы тела. Тот же эффект наблюдался у самок крыс под воздействием Арохлора 1242 в дозе 10 мг/кг массы тела и Арохлора 1016 при поглощении оральной дозы 100 мг/кг ежедневно в течение 21 дня. ПХБФ, вводившиеся крысам в период беременности, могут индуцировать микросомную ферментативную активность в плаценте и у плода, что также случается в печени новорожденных крысят, которые вскармливаются самками, получаю щимн корм с добавлением ПХБФ (Alvares и Kappas, 1975). Benthe и др. (1972b) сообщили, что при воздействии на крыс голодания или холода, остаточные количества ПХБФ, содержащиеся в жировой ткани, высвобождались при мобилизации жира и приводили к увеличению микросомной ферментативной активности клеток печени.
7.4.2 Порфирия
Порфирия печеночной этиологии может быть вызвана рядом ПХБФ (Хлофен А60, Фенохлор DP6, Арохлор 1016, 1242, 1254 и 1260) у цыплят, кроликов, японских куропаток и крыс (Vos и Koeman, 1970; Vos и Beems, 1971; Iverson et al., 1975; Vos et al., 1971; Goldstein et al., 1974, 1975a, 1975b). Индукция порфирина была изучена более интенсивно на крысах. Зависимое от дозы увеличение уровня порфирина в печени наблюдалось у самок крыс, получавших с кормом 21 суточную дозу Арохлора 1242 на уровне 10 и 100 мг/кг массы тела, но не 1 мг/кг массы тела. Самки крыс оказались более чувствительными, чем самцы, а Арохлор 1016 менее эффективным (Iverson et al., 1975). У крыс, получавших с кормом Арохлор 1254 в дозе 100 мг/кг, увеличение индукции порфирина обычно обнаруживалось 2-4 мес спустя после начала воздействия (Goldstein, 1974) и характеризовалось высокими уровнями уропорфиринов в печени и в моче. Нарушение биосинтеза порфирина было поставлено в связь с увеличением содержания фермента, лимитирующего скорость реакции образования порфирина, а именно 6-аминолезулинатсинтазы (КФ2.3.1.37) (Vos et al., 1971; Goldstein, 1974, 1975).
Kawanishi и др. (1973, 1974) показали, что скармливание Канехлора КС 300 и КС 500 крысам в дозе 500 мг/кг вызывает заметное увеличение выделения с мочой копра- и уропорфиринов и выделения с фекалиями протопорфирина. Такого увеличения не было отмечено при скармливании КС 400. Экспериментальная затравка чистыми тетрахлорбифенилами не вызывала появления порфирии. Однако порфирия неизменно появлялась после многократного подкожного введения препарата КС 400 (общая доза 1,8 г) кроликам в течение 55 дней (Miura et al., 1973).
7.4.3 Влияние на метаболизм стероидов
Было показано, что ПХБФ стимулируют активность ферментов, ответственных за обмен стероидов, таких как эстра-диол и андростерон, более эффективно чем ДДТ и ДДЕ (Risebrough et ai., 1968; Lincer a. Peakall, 1970). Было высказано предположение, что воздействие на репродуктивную функцию (см. раздел 7.4) может быть отнесено за счет индукции ферментов, вызвавших метаболизацию стероидов (Kihlstrom et al., 1973). Длительное скармливание Хлофена А60 23-м самкам мышей линии NMRI (суточная доза 0,025 мг) вызвало удлинение эстрального цикла и уменьшение частоты имплантации яйцеклеток (Orberg и Kihlstrom, 1973).
7.4.4 Другие биохимические эффекты
Уровень содержания витамина А в печени, как было показано Villeneuve и др. (1971а), у беременных крольчих под воздействием Арохлора 1254 уменьшается наполовину по сравнению с нормой. Подобные же результаты были получены Cecil и др. (1973) на самцах и самках японских куропаток и на крысах после скармливания им Арохлора 1242 в концентрации 100 мг/кг. Уменьшение содержания витамина А в печени на 50%, обнаруженное у самцов и самок крыс, было также найдено у самок и самцов куропаток при условии, что последние содержались в темноте с целью предотвращения яйцекладки.
Снижение содержания витамина А в печени крыс, получавших с кормом 0,1% ПХБФ (вид ПХБФ не указан), было описано Innami и др. (1974). Крысы, получавшие дополнительно витамин А (3400 ME) наряду с ПХБФ в течение 6 нед, лучше росли по сравнению с животными, получавшими только ПХБФ. У крыс, получавших ПХБФ и корм с дефицитом содержания витамина А, наблюдалась значительная задержка роста. При нахождении на рационе, содержащем ПХБФ, уровень витамина А в печени крыс уменьшался на 20% по сравнению с нормой, что наблюдалось в течение всего экспериментального периода. Обогащение рациона 1000 ME витамина А не восстанавливало уровень его в печени. Однако назначение 3000 ME витамина А вместе с кормом, содержавшим ПХБФ, позволяло восстановить более высокий по сравнению с нормой уровень витамина А в печени. Авторы пришли к заключению, что витамин А может играть определенную роль в детоксикации ПХБФ, что более вероятно, чем предположение о том, что ПХБФ, играет роль в нарушении метаболизма витамина А.
Арохлор 1254, вводившийся внутрибрюшинно крысам в дозе 25 мг/кг массы тела ежедневно в течение 4 дней, вызвал 4-5-кратное повышение экскреции тироксина с желчью в течение 3-часового периода. При этом сильно возрастал феномен просветления желчи. Гипобилирубинемия была получена у крыс Bastomsky и др. (1975), которые исследовали механизм этого явления путем ежедневного внутрибрюшинного введения Арохлора 1254 (20 мг/кг массы тела в кукурузном масле) самкам крыс в течение 4 дней с последующим определением in vitro образования глюкуронида билирубина микросомами клеток печени. Обработка животных ПХБФ не вызывала увеличения UDR-глюкуронозилтрансферазной активности (2.4.1.7). Уровни билирубина в сыворотке также существенно уменьшались под воздействием ПХБФ на крыс линии Gunn, которые имеют генетический дефицит UDP-глюкуроно-зилтрасферазиой активности (2.4.1.7).
7.4.5 Потенцирование и антагонизм при действии ПХБФ
Поскольку ПХБФ могут стимулировать активность микро-сомных ферментов, можно предположить, что они способны потенцировать действие тех химических соединений, которые сами подвергаются микросомной активации, и уменьшать действие других соединений, подвергающихся детоксикации.
Villenuve и др. (1973) продемонстрировал антагонистический эффект, наблюдая феномен уменьшения времени фено-барбиталового сна у крыс, получавших с кормом Арохлор 1242, 1254 и 1260, при отсутствии его у крыс, получавших Арохлор 1221. Johnstone и др. (1974) подтвердили эти наблюдения применением целой серии отдельных соединений ПХБФ. Tanaka и Komatsu (1972) показали, что время гекса-барбиталового сна у самок крыс уменьшалось на 49% по сравнению с контролем при ежедневном поглощении оральной дозы Канехлора 500 2 мг/'кг в течение 3 дней (общая доза 6 мг/кг). Когда суточная доза 0,4 мг/кг давалась в течение 15 дней (общая доза 6 мг/кг), уменьшения указанного времени сна не наблюдалось. Когда же такую небольшую дозу давали в течение 45 и 53 дней, уменьшение времени гексабар-биталового сна оставалось на уровне 12-13%. Phillips не обнаружили потенцирования холинэстеразно-ингибирующего действия паратиона у крыс, получавших Арохлор 1221 и 1254; эти данные не следует рассматривать как свидетельство того, что при этом не было усиления активации паратиона, поскольку одновременно могла происходить стимуляция его детоксикации. Стимуляция детоксикации паратиона, но не его зктивации, была обнаружена в микросомах клеток кроликов (Villeneuve et al., 1971a). Lichtenstein (1972) показал, что ЛХБФ увеличивают токсичность паратиона для мух.
Cecil и др. (1975) показали, что способность ПХТФ вызывать уменьшение времени фенобарбиталового сна у куропаток значительно меньше, чем при воздействии ПХБФ.
Арохлор 1254 при скармливании в концентрации 160 мг/кг в течение 8 нед 5-недельным самцам и самкам крыс линии Fischer-344 уменьшил смертность, вызываемую скармливанием гексахлорофена в концентрации 600 мг/кг, с 77% до 7% и полностью предотвращал появление параличей, которые наблюдались у всех животных, получавших гексахлорофен. Однако у животных, подвергавшихся комбинированной обработке, все-таки наблюдались гистологические изменения в мозге, характерные для гексахлорофена, что не исключает возможности отдаленных проявлений токсичности за пределами 8-недельного срока эксперимента. Защитный эффект Арохлора 1254 был объяснен его способностью к детоксикации посредством индукции микросомной ферментативной активности клеток печени (Jones et al., 1974).
7.5 Цитотоксические эффекты
Peakall и др. (1972) обнаружили значительное увеличение числа случаев хромосомных аномалий у эмбрионов голубей при скармливании родителям Арохлора 1254 в концентрации 10 мг/кг. Nilsson и Ramel (1974) не выявили никаких хромосомных нарушений у мух Drosophila melanogaster при добавлении к субстрату Хлофена АЗО или А50. Green и др. (1975) вводили Арохлор 1242 per os крысам в виде однократных доз в 1250, 2500 и 5000 мг/кг или же повторных доз в 500 мг/кг/ день в течение 4 дней. Арохлор 1254 также вводили в течение 5 дней в дозах 75, 150 и 300 мг/кг/день. Мутагенное действие, о чем судили по цитогенетическим сдвигам в костном мозге и сперматогониях, при этом обнаружено не было.
7.6 Подавление иммунитета
Введение ПХБФ приводит к атрофии лимфоидной ткани цыплят (Flick et al., 1965; Vos Koeman, 1970), фазанов (Dahlgren et al., 1972) и кроликов (Vos и Beems, 1971). Vos и de Roij (1972) и Vos и van Drielgrootenhuis (1972) пришли к заключению, что наблюдаемый эффект может быть отнесен за счет иммунодепрессивного действия ПХБФ. Они нашли, что при иммунизации морских свинок, получавших с кормом Хлофен А60 или Арохлор 1260 в концентрации 50 мг/кг, столбнячным анатоксином, у животных обнаруживается более низкий титр антитоксина и меньшее число антитоксинпродуци-рующих клеток по сравнению с морскими свинками контрольной группы, что сопровождается значительным уменьшением уровня иммуноглобулинов. Кожная туберкулиновая реакция (как параметр клеточного иммунитета) у морских свинок, иммунизированных полным адьювантом Фрейнда, была также снижена при скармливании этих препаратов в концентрации 50 мг/кг. Vos и de Roij (1972) высказали предположение, что способность ПХБФ увеличивать чувствительность утят к вирусу утиного гепатита (Friend и Trainer, 1970) и рыб к грибковым заболеваниям (Hansen et al., 1971) может быть связана с иммунодепрессивным эффектом.
Kimuru и Baba (1973) обнаружили повышение частоты пневмоний, легочных и внутричерепных абсцессов у крыс, получавших корм, содержащий Канехлор 400, и высказали предположение, что это объясняется снижением сопротивляемости к инфекции.
7.7 Влияние на репродуктивную функцию
При изучении репродукции на протяжении одной генерации крысам скармливали Арохлор 1242, 1254 или 1260 в концентрации 1, 10 и 100 мг/кг. Воздействие Арохлора 1242 и 1254 в концентрации 100 мг/кг приводило к понижению выживаемости новорожденных крысят. При использовании Арохлора 1260 никакого влияния на репродукцию обнаружено не было (Keplinger et al., 1971). В исследованиях на двух генерациях (binder et al., 1974) крысам скармливали Арохлор 1254 в концентрации 0, 1, 5, 20 и 100 мг/кг, Арохлор 1260 в концентрации 0, 5, 20 и 100 мг/кг. Крысы, подвергшиеся воздействию Арохлора 1254 в концентрации 20 мг/кг и выше, имели меньшее число новорожденных в помете. Арохлор 1260 не оказывал никакого влияния на репродуктивную функцию даже в концентрации 100 мг/кг. Kihlstrom и др. (1973) показали, что суточная пероральная доза в 25 мкг Хлофена А60, вводимая самкам мышей в течение 62 дней, существенно увеличивает продолжительность эстрального цикла и уменьшает частоту имплантации яйцеклеток. Для изучения влияния ПХБФ на формирование половых функций в раннем постнатальном периоде они также скрещивали мышей, которые вскармливались самками, получавшими Хлофен А60 в течение лактационного периода. В тех случаях, когда оба родителя вскармливались молоком, содержащим ПХБФ, имело место снижение частоты имплантации яйцеклеток.
У обезьян резус Allen (1975) отметил более низкую фертильность и уменьшение массы тела новорожденных после скармливания рациона, содержащего Арохлор 1248 в концентрации 2,5 мг/кг, в течение нескольких месяцев.
Опыты Aulerich и др. (1971) и Kinger и др. (1972) показали, что Арохлор 1254, скармливавшийся норкам в концентрации 5 мг/кг, оказывает выраженное неблагоприятное воздействие на репродуктивную функцию.
Было опубликовано несколько сообщений о том, что ПХБФ могут необлагоприятно влиять на продукцию яиц и на вылупляемость птенцов. Контаминация кормов ПХБФ, произошедшая через теплообменник, послужила причиной уменьшения вылупляемости куриных яиц на одной из крупных птицефабрик в США (Kolbye, 1972), что было подтверждено и в лабораторных исследованиях. Keplinger и др. (1971) обнаружили сниженную вылупляемость яиц при добавлении в рацион кур-несушек Арохлора 1242 в концентрации 10 мг/кг или Арохлора 1254 в концентрации 100 мг/кг; такого явления не наблюдалось при использовании Арохлора 1260 в концентрации 100 мг/кг. Неблагоприятное воздействие на яйца было отмечено при использовании Арохлора 1249 в концентрации Ю мг/кг (Panel on Hazardous Trace Substances, 1972). Peakall и др. (1972) скармливали голубям Арохлор 1254 в концентрации 10 мг/кг в течение 3 мес и не обнаружили заметного уменьшения вылупляемости яиц 6 мес спустя вследствие повышения смертности эмбрионов.
Жизнеспособность икры семги зависела в определенной степени от содержания в ней ПХБФ; Johansson и др. наблюдали (1970) 12% смертность икринок, содержащих ПХБФ на уровне 9,2 мг/кг в экстрагируемом жире, и 100% гибель при увеличении этого содержания до 34 мг/кг. Отрицательное влияние на репродуктивную функцию водных беспозвоночных можно было наблюдать при концентрации ПХБФ в воде порядка 5 мкг/л.
Потенциальный тератогенный эффект ПХБФ изучали путем затравки беременных самок в течение беременности. У потомства крыс, получавших суточные дозы Арохлора 1242, 1254 и 1260 на уровне 10 и 30 мг/кг (Keplinger et al., 1971) или Арохлора 1254 в дозе 100 мг/кг (Villeneuve et al., 1971b), и кроликов, получавших Арохлор 1254 в дозах 10 и 50 мг/кг (Villeneuve et al., 1971b), никаких отклонений от нормы не наблюдалось. Инъекции ПХБФ в полость яиц приводили к нарушению строения клюва у цыплят (McLaughlin et al., 1963). Cecil и др. (1974) заявили, что скармливание Арохлора 1242 и 1254 курам в концентрации 20 мг/кг вызывает тератогенный эффект и уменьшение вылупляемости оплодотворенных яиц.
7.8 Неоплазия и аденофиброз
Печень является единственным органом, поражаемым опухолями в результате поглощения ПХБФ. Но и др. (1973) скармливали группам из 12 самцов мышей линии dd рацион, содержавший 500, 250, 100 и 0 мг/кг Канехлора 500, 400 и 300 соответственно. Через год у 7/12 мышей появились неопластические или гиперпластические узелки и у 5/12 - карцинома печени; все эти явления наблюдались у мышей, получавших корм, содержавший 500 мг/кг Канехлора 500. Метастазы при этом не наблюдались. Во втором исследовании, проведенном на мышах, комбинированное воздействие Канехлора 500 и а- или р-изомеров гексахлорциклогексана приводило к увеличению частоты развития неопластических (или гиперпластических) узелков и карциномы печени. Комбинация из Канехлора 500 и у-гексахлорцик-логексана не вызывала образования опухолей. Добавление к корму одного Канехлора 500 в концентрации 250 мг/кг и (3-или у-гексахлорциклогексана в концентрации 250, 100 или 50 мг/кг не вызывало появления опухолей. Однако а-гексахлорциклогексан вызвал у 8/30 животных появление карциномы печени и у 23/30 мышей гиперпластических узелков.
Группа из 50 инбредных самцов мышей линии BALB/g получала рацион, содержавший Арохлор 1254 в концентрации 0 или 300 мг/кг (49,8 мг/кг массы тела), в течение 6 и 11 мес соответственно. У выживших 58 контрольных животных опухолей печени не отмечалось. 10 случаев гепатом (неопластические и гиперпластические узелки) были отмечены у 9/22 выживших мышей, получавших корм с добавлением Арохлора 1254 в течение 11 мес, и у 1/24 из выживших мышей, получавших Арохлор 1254 в течение 6 мес. Кроме того, наблюдался аденофиброз (холангиофиброз) в печени всех 22 мышей, получавших Арохлор 1254 в течение 11 мес при отсутствии его в других группах (Kimbrough и binder, 1974).
В другом исследовании (Kimbrough et al., 1975) 200 самок крыс линии Sherman, выведенных методом COBS - рандомизации (потомки линии Osborne Mendel), получали рацион, содержавший Арохлор 1260 в концентрации 100 мг/кг (11,6 - 4,3 мг/кг массы тела) около 21 мес; 200 самок крыс содержали в качестве контрольной группы. Крысы были забиты в. возрасте 23 мес. Карцинома печени была обнаружена у 25/184 животных опытной группы и у 1/173 - контрольной группы. У 144/184 опытных животных были обнаружены неопластические (или гиперпластические) узелки при отсутствии их в контроле. Участки гепатоциллюлярной альтерации были обнаружены у 28/174 контрольных и у 182/184 опытных животных. Арохлор не оказывал никакого влияния на возникновение опухолей в других органах и частоту метастазирования опухолей печени. В этом и в двух более ранних исследованиях аденофиброз печени наблюдался у самцов и самок крыс, получавших с кормом Арохлор 1260 или 1254 (Kimbrough et al., 1972, 1973, 1975). Аденофиброз печени является стойким и прогрессирующим поражением, выражающимся в отчетливой пролиферации фиброзной ткани и эпителиальных железистых клеток, которые хорошо дифференцированы у мышей, будучи атипичными у крыс.
В ходе предварительного исследования было показано, что опухоли печени (множественные аденоматозные узелки) были вызваны Канехлором 400 у 6/10 самок, но не у самцов крыс линии Donryu. Длительность скармливания Канехлора в ходе исследования варьировала, а число животных, использовавшихся в опытах, было небольшим (10 опытных и 5 контрольных крыс каждого пола) (Kimura и Baba, 1973). Makiura и др. (1974) сообщили, что ПХБФ (Канехлор 500) подавляли развитие опухолей печени у самцов крыс линий Sprague-Dawley под воздействием известных канцерогенов З'-метил-/0-диметиламиноазобензола, N-2-флюоросенилацетамида и ди-этилнитрозамина.